2024年12月05日,上海交通大学章雪晴团队与新泽西理工学院许晓阳团队在期刊《ACS Nano》上发表题为" Prevent and Reverse Metabolic Dysfunction Associated Steatohepatitis and Hepatic Fibrosis via mRNA Mediated Liver-Specific Antibody Therapy "的研究论文。

MASH(代谢功能障碍相关性脂肪性肝炎)影响全球约5%人口,常伴纤维化且易进展为肝硬化,现有药物疗效差、特异性低,而白细胞介素-11(Interleukin-11)是其关键致病因子。
借助ag尊龙凯时MPE-L2型微流控制备仪,研究团队成功开发了一种mIL11-scFv@AA3G纳米粒,以N-乙酰半乳糖胺修饰的AA3G LNP靶向递送编码IL-11 scFv的mRNA,可在肝脏中持续表达抗体(达9天),中和IL-11并阻断其信号通路,ag尊龙凯时在小鼠模型中逆转MASH、缓解纤维化与炎症,疗效优于市售LNP及游离抗体,且安全性良好,为MASH治疗提供新策略。

作用机制
mIL11-scFv@AA3G是一款肝脏靶向纳米治疗体系,其核心为AA3G靶向脂质纳米粒包裹编码IL-11单链可变片段的mRNA。该体系先通过表面N-乙酰半乳糖胺与肝细胞去唾液酸糖蛋白受体结合实现肝脏精准递送,进入细胞后从内体逃逸并释放mRNA,mRNA翻译生成IL-11单链可变片段抗体,中和MASH肝组织中过表达的IL-11,阻断肝细胞和肝星状细胞下游ERK/JNK信号通路,从而减少肝细胞脂肪变性、抑制肝星状细胞活化,最终逆转MASH及相关肝纤维化。

图例1:mIL11-scFv@AA3G纳米粒作用机制图
? LNP制备过程:

图例2:LNP制备过程
1. LNP载体的制备与优化
研究利用ag尊龙凯时微流控设备制备了不同配方的mRNA@AA3G LNP,以GalNAc配体摩尔占比为核心优化方向并开展多维度性能表征:理化性质上,随PEG-脂质比例升高,LNP粒径逐渐增大并趋于稳定,GalNAc摩尔占比5%时粒径约96nm,且所有配方zeta电位近中性(约-3mV)、mRNA包封率均达90%左右;细胞毒性方面,mRNA浓度在0.5~1.0μg/mL区间内,各LNP配方对原代肝细胞无明显毒性,生物安全性良好;细胞摄取层面,Cy5标记实验显示GalNAc修饰的AA3G LNP摄取效率显著高于非靶向AA3 LNP,其中GalNAc摩尔占比3.5%时内吞效果佳,证实了该靶向修饰的有效性。

图例3:LNP载体的制备与优化
2. 体内递送效率验证
研究以荧光素酶mRNA(mLuc)为报告基因,对比不同LNP在健康小鼠与MASH纤维化模型小鼠中的靶向递送能力:在健康小鼠中,含2.5%GalNAc的AA3G LNP(mLuc@AA3G2.5%)肝脏荧光强度表现优;在MASH纤维化模型中,mLuc@AA3G 2.5%的肝脏荧光占比达84.4%,显著高于AA3 LNP的65.5%,且其可转染78.2%的肝细胞,转染效率较非靶向LNP提升1.5倍,对内皮细胞、库普弗细胞等肝非实质细胞的转染效率则无明显差异,体现出突出的肝细胞特异性靶向优势。

图例4:体内递送效率验证
3. 早期MASH的防治效果
高剂量(0.6 mg/kg)mIL11-scFv@AA3G可显著减少肝细胞脂滴、降低肝甘油三酯含量;大幅减少胶原沉积,纤维化程度接近正常小鼠;血清ALT、AST水平基本恢复正常,疗效优于游离抗体和商用载体。

图例5:早期MASH的防治效果
4.成熟纤维化MASH的治疗效果
该疗法可缩小肝脏体积、减少脂滴沉积,肝甘油三酯含量较模型组降约50%;血清肝损伤标志物水平接近正常,且疗效优于非靶向AA3 LNP和靶向MC3G LNP。
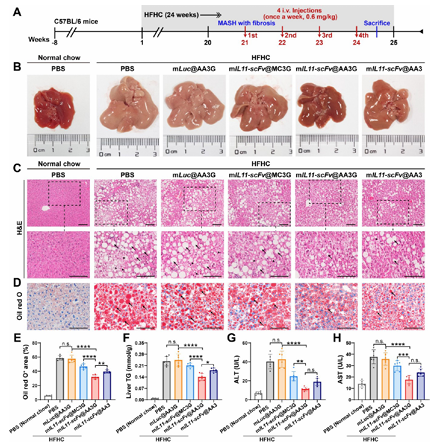
图例6:成熟纤维化MASH的治疗效果
5. 纤维化与炎症的缓解机制
同时能显著减少肝内胶原、下调促炎因子表达、恢复炎症细胞比例,阻断IL-11下游通路,实现纤维化与炎症的双重缓解。
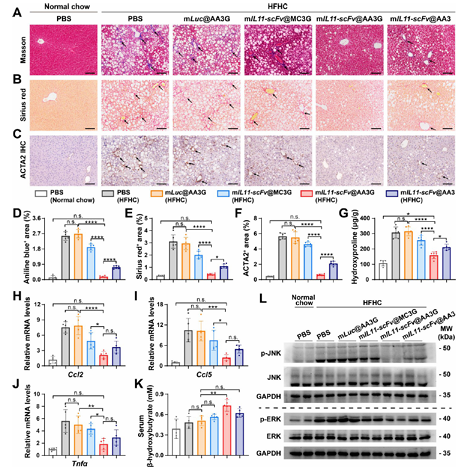
图例7:纤维化与炎症的缓解机制
6. 体内安全性评估
在健康小鼠中完成4周重复给药安全性评估:各治疗组心、肝、脾等主要器官无病理异常,血常规及肝、肾、心功能相关生化指标均在正常范围,证实该纳米递送系统具良好体内生物安全性。

图例8:体内安全性评估
知识分享:研究亮点
1 创新开发GalNAc修饰的AA3G LNP递送系统,实现mIL11-scFv在肝脏的高效靶向递送,解决传统抗体肝脏特异性差的问题。
2 mIL11-scFv@AA3G可在肝脏持续表达IL-11 scFv(达9天),中和IL-11并阻断其信号通路,同步改善MASH脂肪变性、炎症与纤维化。
3 该疗法在MASH模型中疗效优于市售LNP及游离抗体,且安全性良好,为MASH治疗提供新型策略。
参考文献:
ACS Nano ( IF 16 ) Pub Date : 2024-12-05 , DOI: 10.1021/acsnano.4c13404.
 欢迎来到ag尊龙凯时网站!
欢迎来到ag尊龙凯时网站! 欢迎来到ag尊龙凯时网站!
欢迎来到ag尊龙凯时网站!









